私たちの研究室では、レオウイルス目に属するウイルス(ロタウイルス、哺乳類レオウイルス、コウモリ由来レオウイルス等)に加え、カリシウイルス科のノロウイルスの研究も推進しています。
ロタウイルスの人工合成法を用いた分子生物学的解析
ロタウイルスはヒトに重篤な下痢を引き起こし、レオウイルス科の中でも最も重要なウイルスの一つです。 ロタウイルスは11分節の2本鎖RNAをゲノムとして持ちます。ロタウイルスは病原性の解析やワクチン開発の観点から、人工合成法(リバースジェネティクス系)の開発が試みられてきましたが、多くの研究者たちの長年の努力にも関わらず、完全なcDNAに由来するロタウイルスの遺伝子操作系は確立されておりませんでした。私たちの研究室は哺乳類レオウイルスやコウモリレオウイルスの研究で得られた知見から、ロタウイルスの人工合成法の開発に成功しました。現在は、この技術を用いたロタウイルスの解析を行っています。
Rotaviruses are a leading cause of severe diarrhea in humans and are among the most important viruses within the family Reoviridae. Rotaviruses possess an eleven-segmented double-stranded RNA genome. Owing to their medical significance, extensive efforts have been made to develop reverse genetics systems for rotaviruses to facilitate studies of viral pathogenicity and vaccine development. However, despite decades of research by many investigators, a robust genetic manipulation system based entirely on cloned cDNA had not been established. Building on insights gained from studies of mammalian orthoreoviruses and bat-borne reoviruses, our laboratory successfully developed a synthetic (reverse genetics) system for rotaviruses. We are currently utilizing this platform to conduct comprehensive molecular and virological analyses of rotavirus infection.
ノロウイルスの人工合成法を基盤とした増殖機構・病原性の解析
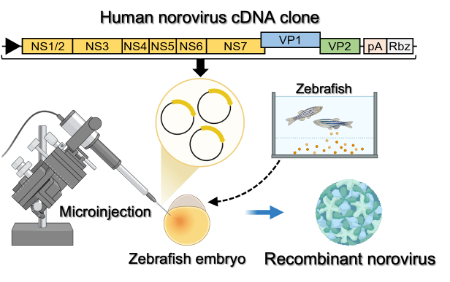
ノロウイルスは急性胃腸炎を引き起こすウイルスであり、感染者数の多さや社会的損失の大きさから、最も重要な腸管感染症原因ウイルスの一つとされています。しかし、有効なワクチンや治療薬の開発はいまだ十分に進んでいません。その要因の一つとして、ノロウイルス研究に不可欠である効率的な培養系の確立や、人工合成系(リバースジェネティクス系)の開発が遅れていることが挙げられます。近年、ヒト腸管オルガノイドを用いた培養系が報告されていますが、技術的・コスト的制約に加え、ウイルス増殖効率の面でも課題があります。一方で、小型魚類であるゼブラフィッシュが、ノロウイルス研究に有用な新たなモデル生物として注目されています。こうした知見を踏まえ、本研究室ではゼブラフィッシュを用いたノロウイルスのリバースジェネティクス系を開発しました。現在は、この技術を基盤として、ノロウイルスの増殖機構や病原性の解析を進めています。
Noroviruses are a major cause of acute gastroenteritis and are regarded as one of the most important etiological agents of enteric infections due to their high incidence and substantial socioeconomic burden. However, the development of effective vaccines and antiviral therapies for noroviruses remains limited. One contributing factor is the delayed establishment of experimental platforms essential for norovirus research, including efficient culture systems and synthetic approaches such as reverse genetics systems. In recent years, culture systems based on human intestinal organoids have been reported; however, these models face technical and cost-related limitations and often exhibit suboptimal viral replication efficiency. In contrast, zebrafish, a small vertebrate model organism, have attracted attention as a promising new experimental model for norovirus research. Building on these advances, our laboratory has developed a reverse genetics system for noroviruses using zebrafish. We are currently utilizing this platform to investigate the mechanisms of norovirus replication and pathogenesis.
哺乳類レオウイルスによる抗腫瘍剤の開発 / Oncolytic viral therapy using reovirus
哺乳類レオウイルス(MRV)は、10分節の2本鎖RNAをゲノムとして保持し、レオウイルス科のモデルウイルスとして研究されています。MRVはRasの活性化変異に起因する腫瘍細胞で選択的に増殖し、腫瘍細胞を溶解することから、頭頚部癌、大腸癌、乳癌、すい臓癌等の治療を目的とした、腫瘍溶解性ウイルスとしての研究が進んでいます。MRVの癌治療研究は、これまで野生型のMRVを用いておこなわれてきましたが、殺腫瘍効果の観点から改良が望まれています。私たちはMRVで応用が困難であったウイルス遺伝子の改変技術(リバースジェネティクス系)を導入・駆使することで、遺伝子改変MRVを作出し、より安全で治療効果の高い腫瘍溶解性MRVの開発研究を行っています。
Mammalian orthoreoviruses (reoviruses) are members of the family Reoviridae and contain a genome consisting of 10 segments of double-stranded (ds)RNA. Reoviruses are highly tractable experimental models for studies of dsRNA virus replication and pathogenesis. In the last decade, the potential of reoviruses as oncolytic agents against various tumors, including head and neck, colon, breast and pancreatic cancers, has been investigated in animal models and humans. The putative oncolytic potential of reoviruses is based on the observation that reoviruses induce cell death and apoptosis in tumor cells with an activated Ras signaling pathway. However, while wild-type reovirus-based oncolytic therapies have been safe, the efficacy so far is limited. We are thus using genetic modification to develop safer and more effective reovirus-based cancer therapeutics
コウモリ由来高病原性レオウイルス / Highly pathogenic bat reovirus
コウモリはSARSコロナウイルス、ニパウイルス、エボラウイルス、狂犬病ウイルスなど多くの致死的感染を引き起こす人獣共通感染症のレゼルボアとして注目されています。1968年にコウモリから分離されたPteropine orthoreovirus(PRV)についてはこれまでヒトや動物の疾患との関連性は報告されていませんでしたが、2007年、東南アジアで重篤な呼吸器疾患を呈した患者においてPRV感染(Melaka株)が始めて報告されました。この報告以降、他のアジア諸国においても同様の感染者が相次いで報告され、日本国内においては私達のグループが東南アジアから帰国後重篤な呼吸器症状を呈した患者からPRVの分離を行いました。これらの報告はコウモリを起源とするレオウイルスが種の壁を越えヒトに感染伝播した結果と推察され、新興感染症としてのPRVの感染制御基盤の確立が望まれています。私たちはPRVにおける予防・治療法の確立を目指しPRVの複製機構、病態発現機序の解明を行っています。
Bats are a natural reservoir for many important zoonotic viruses, including Hendra virus, Nipah virus and potentially SARS coronavirus and Ebola virus. In 1968, the Pteropine orthorevirus (PR) was isolated from flying fox. While it was not associated with and human disease, Melaka virus which is genetically similar to PRVB was recently isolated from a human patient in Malaysia with acute respiratory tract infection (RTI). Subsequently, other related strains of bat-associated orthreoviruses have been isolated in Malyasia, Indonesia and China. We also isolated and characterized another new PRV, Miyazaki-Bali/2007 virus from a patient with acute RTI after returning to Japan from Indonesia in 2007. These isolates have given rise to increasing concern about bat-transmitted orthoreovirus infection in humans. We are investigating how PRV replicates and causes disease by using a combination of genetic biochemical and biophysical approaches. Our aim is ultimately to develop vaccines, diagnostics and therapeutics for bat reovirus-related diseases.
